Тест по химии Химические уравнения 8 класс с ответами. Тест содержит 2 части. В части 1 — 15 заданий базового уровня. В части 2 — 3 задания повышенного уровня.
Часть 1
1. Верны ли следующие суждения?
А. Масса реагентов равна массе продуктов реакции.
Б. Химическое уравнение — условная запись химической реакции с помощью химических формул и математических знаков.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
2. В ходе химической реакции число атомов некоторого элемента
1) только увеличивается
2) только уменьшается
3) не изменяется
3. В ходе химической реакции число молекул реагентов
1) только увеличивается
2) только уменьшается
3) не изменяется
4) может как увеличиваться, так и уменьшаться
4. В ходе химической реакции число молекул продуктов реакции
1) только увеличивается
2) только уменьшается
3) не изменяется
4) может как увеличиваться, так и уменьшаться
5.
СН 4 + O 2 → СO 2 + Н 2 O.
1) 5
2) 6
3) 7
4) 8
6.
Составьте уравнение реакции по схеме:
FeS + O 2 → Fe 2 O 3 + SO 2 .
1) 13
2) 15
3) 17
4) 19
7.
Составьте уравнение реакции по схеме:
Nа 2 O + Н 2 O → NaOH.
1) 4
2) 5
3) 6
4) 7
8.
Составьте уравнение реакции по схеме:
Н 2 O + N 2 O 5 → HNO 3 .
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
9.
Составьте уравнение реакции по схеме:
NаОН + N 2 O 3 → NaNO 2 + Н 2 O.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
10.
Составьте уравнение реакции по схеме: Аl 2 O 3 + HCI → AlCl 3 + Н 2 O.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 10
2) 11
3) 12
4) 14
11.
Составьте уравнение реакции по схеме:
Fe(OH) 3 + H 2 SO 4 → Fe 2 (SO 4) 3 + Н 2 O. Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 12
2) 13
3) 14
4) 15
12. Составьте уравнение реакции по схеме:
гидроксид меди (II) + соляная кислота → хлорид меди (II) + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
13. Составьте уравнение реакции по схеме:
гидроксид алюминия → оксид алюминия + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 4
2) 5
3) 6
4) 7
14. Составьте уравнение реакции по схеме:
оксид железа (III) + водород → железо + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 6
2) 7
3) 8
4) 9
15. Составьте уравнение реакции по схеме:
карбонат кальция + соляная кислота → хлорид кальция + вода + оксид углерода (IV).
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 6
2) 7
3) 8
4) 9
Часть 2
1. Установите соответствие между исходными веществами и продуктами соответствующих химических реакций. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту.
Исходные вещества
А) Н 2 + O 2 →
Б) С 2 Н 6 + O 2 →
В) Al(OH) 3 + H 2 SO 4 →
Г) Ca(NO 3) 2 + Na 3 PO 4 →
Продукты реакции
1) СО 2 + Н 2 О
2) Н 2 О
3) Са 3 (РО 4) 2 + NaNO 3
4) Al 2 (SO 4) 3 + Н 2 О
2. Установите соответствие между схемой реакции и суммой коэффициентов в уравнении реакции. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту.
Уравнения реакций
А) Fe 3 O 4 + Аl → Аl 2 O 3 + Fe
Б) Р 2 O 5 + Н 2 О → Н 3 РO 4
В) Al + O 2 → Аl 2 O 3
Г) Fe(OH) 3 → Fe 2 O 3 + Н 2 О
Сумма коэффициентов
1) 6
2) 9
3) 12
4) 18
5) 24
3. Закон сохранения массы вещества является частью более общего закона сохранения материи. Виды материи (энергия и вещество) взаимосвязаны по формуле Эйнштейна: ΔЕ = Δm ⋅ с 2 (где скорость света с = 3 ⋅ 10 8 м/с). Если в ходе реакции, например, выделилось ΔЕ = 90 кДж = 9 ⋅ 10 4 Дж энергии, то масса системы уменьшилась на величину: Δm = ΔЕ/с 2 = 9 ⋅ 10 4 /(3 ⋅ 10 8) 2 = 10 -12 кг = 10 -9 г. Эта величина меньше, чем точность аналитических весов (10 -6 г). Поэтому изменениями массы в ходе химических реакций можно пренебречь. Вычислите величину выделившейся энергии ΔЕ в кДж, если масса системы в ходе реакции уменьшилась на 2,5 ⋅ 10 -9 г. В ответе запишите величину ΔЕ без указания единиц измерения.
Ответы на тест по химии Химические уравнения 8 класс
Часть 1
1-3
2-3
3-2
4-1
5-2
6-3
7-1
8-4
9-2
10-3
11-1
12-2
13-3
14-4
15-1
Часть 2
1-2143
2-5121
3-225
Чтобы пользоваться предварительным просмотром презентаций создайте себе аккаунт (учетную запись) Google и войдите в него: https://accounts.google.com
Подписи к слайдам:
ОГБОУ «Смоленская специальная(коррекционная)общеобразовательная школа 1 и 2 видов»(Центр дистанционного образования) Химические уравнения урок химии,8класс, УМК О.С.Габриелян
Вспомните на какие две группы делятся все явления, происходящие с телами и веществами?
Какие признаки химических реакций вы знаете?
Какие условия должны выполняться,чтобы произошла химическая реакция? Необходимо,чтобы реагирующие вещества соприкоснулись. Нагревание. Электрический ток или свет.
“ Все изменения,которые случаются в действительности,находятся в таком состоянии,что сколь от одного тела отнимается,столько прибавляется к другому,так что где убудет немного материи,то умножится в другом месте” М.В.Ломоносов(1756г)
Современная формулировка закона сохранения массы веществ: Масса веществ,вступивших в химическую реакцию,равна массе веществ,получившихся в результате её.
На основании закона сохранения массы веществ составляют уравнения химических реакций
Запишите уравнение: железо+сера=сульфид железа(II) Fe+S=FeS
Алгоритм расстановки коэффициентов в уравнениях химических реакций Подсчитать количество атомов каждого элемента в правой и левой части уравнения химической реакции. Определить, у какого элемента количество атомов меняется, найти НОК. Разделить НОК на индексы – получить коэффициенты. Поставить их перед формулами. Пересчитать количество атомов, при необходимости действие повторить. Последним проверить количество атомов кислорода.
Расставьте коэффициенты в уравнениях химических реакций: 1) KCLO 3 →KCL+O 2 2) Na+Cl 2 →NaCl 3) KNO 3 →KNО 2 +O 2 4) H 2 O+SO 3 →H 2 SO 4 5) Al+S→Al 2 S 3 6) H 2 O 2 →H 2 O+O 2 7) Rb 2 O+H 2 O→RbOH 8) Ba+O 2 →BaO
Домашнее задание: параграф 27 стр139-145,упражнение1; расставьте коэффициенты в уравнениях реакций: P + Cl 2 → PCl 5 Na + S → Na 2 S HCl + Mg → MgCl 2 + H 2 N 2 + H 2 → NH 3 H 2 O → H 2 + O 2
Список литературы: О.С.Габриелян Учебник «Химия 8класс» Дрофа:М;2008г; О.С.Габриелян,Н.П.Воскобойникова,А.В.Яшукова «Химия 8класс».Настольная книга учителя.Дрофа:М;2008г Интернет-ресурсыHttp://shola.ostriv.in.ua/publication/ Http://pedsovet.su/ Http://ru.wikipedia.org/
По теме: методические разработки, презентации и конспекты
Презентация к уроку геометрии 8 класс. Тема: "Площадь квадрата, прямоугольника, параллелограмма"
Вычеслениее площедей являеться составной частью умения решать геометрические задачи. Поэтому основное внимане в своей работе уделяю формираванию практических навыков вычесления площадей в ходе решения...
В уроке 13 «» из курса «Химия для чайников » рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
В результате реакции горения метана CH 4 в кислороде O 2 образуются диоксид углерода CO 2 и вода H 2 O. Эта реакция может быть описана химическим уравнением :
- CH 4 + O 2 → CO 2 + H 2 O (1)
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O 2 расходуется в расчете на 1 молекулу CH 4 и сколько молекул CO 2 и H2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
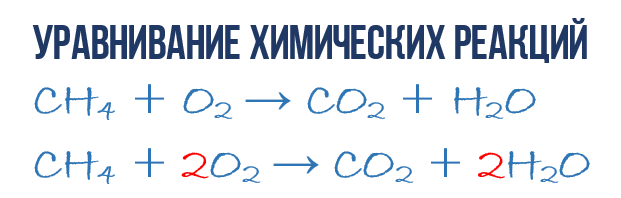
Начнем с углерода. В левой части один атом С входит в состав молекулы CH 4 , а в правой части один атом С входит в состав CO 2 . Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
- 1CH 4 + O 2 → 1CO 2 + H 2 O (2)
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H 4 = 4H) в составе молекулы CH 4 , а в правой – всего 2 атома H в составе молекулы H 2 O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H 2 O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
- 1CH 4 + O 2 → 1CO 2 + 2H 2 O (3)
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H 2 O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H 2 O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
- 1CH 4 + 2O 2 → 1CO 2 + 2H 2 O или СH 4 + 2O 2 → CO 2 + 2H 2 O (4)
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C 7 H 5 N 3 O 6 энергично соединяется с кислородом, образуя H 2 O, CO 2 и N 2 . Запишем уравнение реакции, которое будем уравнивать:
- C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (5)
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
- 2C 7 H 5 N 3 O 6 + O 2 → 14CO 2 + 5H 2 O + 3N 2 (7)
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O 2 . Таким образом полное химическое уравнение будет иметь вид:
- 2C 7 H 5 N 3 O 6 + 10,5O 2 → 14CO 2 + 5H 2 O + 3N 2 (8)
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
- 4C 7 H 5 N 3 O 6 + 21O 2 → 28CO 2 + 10H 2 O + 6N 2 (9)
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
- C 7 H 5 N 3 O 6 + 5,25O 2 → 7CO 2 + 2,5H 2 O + 1,5N 2 (10)
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты , а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро N A =6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O 2 с образованием 28 молей CO 2 , 10 молей H 2 O и 6 молей N 2 .
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O2 = 31,999 г/моль
- CO2 = 44,010 г/моль
- H2 O = 18,015 г/моль
- N2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO 2 , 10·18,015 г = 180,15 г H 2 O и 6·28,013 г = 168,08 г N 2 . Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO2 | |
| 671,98 г CO2 | 180,15 г H2 O | |
| 168,08 г N2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2 :
- CaCO 3 + 2HCl → CaCl 2 + CO 2 + H 2 O (11)
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO 3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 . Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO 3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl 2 (110,99 г/моль), CO 2 (44,01 г/моль) и H 2 O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO 3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
- CaCO 3 (тв.) + 2H + (водн.) → Ca 2+ (водн.) + CO 2 (г.) + H 2 O(ж.) (12)
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO 3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO 2 и H 2 O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений » вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.
Методика решения задач по химии
При решении задач необходимо руководствоваться несколькими простыми правилами:
- Внимательно прочитать условие задачи;
- Записать, что дано;
- Перевести, если это необходимо, единицы физических величин в единицы системы СИ (некоторые внесистемные единицы допускаются, например литры);
- Записать, если это необходимо, уравнение реакции и расставить коэффициенты;
- Решать задачу, используя понятие о количестве вещества, а не метод составления пропорций;
- Записать ответ.
В целях успешной подготовки по химии следует внимательно рассмотреть решения задач, приводимых в тексте, а также самостоятельно решить достаточное число их. Именно в процессе решения задач будут закреплены основные теоретические положения курса химии. Решать задачи необходимо на протяжении всего времени изучения химии и подготовки к экзамену.
Вы можете использовать задачи на этой странице, а можете скачать хороший сборник задач и упражнений с решением типовых и усложненных задач (М. И. Лебедева, И. А. Анкудимова): скачать .
Моль, молярная масса
Молярная масса – это отношение массы вещества к количеству вещества, т.е.
М(х) = m(x)/ν(x), (1)
где М(х) – молярная масса вещества Х, m(x) – масса вещества Х, ν(x) – количество вещества Х. Единица СИ молярной массы – кг/моль, однако обычно используется единица г/моль. Единица массы – г, кг. Единица СИ количества вещества – моль.
Любая задача по химии решается через количество вещества. Необходимо помнить основную формулу:
ν(x) = m(x)/ М(х) = V(x)/V m = N/N A , (2)
где V(x) – объем вещества Х(л), V m – молярный объем газа (л/моль), N – число частиц, N A – постоянная Авогадро.
1. Определите массу иодида натрия NaI количеством вещества 0,6 моль.
Дано : ν(NaI)= 0,6 моль.
Найти : m(NaI) =?
Решение . Молярная масса иодида натрия составляет:
M(NaI) = M(Na) + M(I) = 23 + 127 = 150 г/моль
Определяем массу NaI:
m(NaI) = ν(NaI) M(NaI) = 0,6 150 = 90 г.
2. Определите количество вещества атомного бора, содержащегося в тетраборате натрия Na 2 B 4 O 7 массой 40,4 г.
Дано : m(Na 2 B 4 O 7)=40,4 г.
Найти : ν(B)=?
Решение . Молярная масса тетрабората натрия составляет 202 г/моль. Определяем количество вещества Na 2 B 4 O 7:
ν(Na 2 B 4 O 7)= m(Na 2 B 4 O 7)/ М(Na 2 B 4 O 7) = 40,4/202=0,2 моль.
Вспомним, что 1 моль молекулы тетрабората натрия содержит 2 моль атомов натрия, 4 моль атомов бора и 7 моль атомов кислорода (см. формулу тетрабората натрия). Тогда количество вещества атомного бора равно: ν(B)= 4 ν (Na 2 B 4 O 7)=4 0,2 = 0,8 моль.
Расчеты по химическим формулам. Массовая доля.
Массовая доля вещества – отношение массы данного вещества в системе к массе всей системы, т.е. ω(Х) =m(Х)/m, где ω(X)– массовая доля вещества Х, m(X) – масса вещества Х, m – масса всей системы. Массовая доля – безразмерная величина. Её выражают в долях от единицы или в процентах. Например, массовая доля атомного кислорода составляет 0,42, или 42%, т.е. ω(О)=0,42. Массовая доля атомного хлора в хлориде натрия составляет 0,607, или 60,7%, т.е. ω(Cl)=0,607.
3. Определите массовую долю кристаллизационной воды в дигидрате хлорида бария BaCl 2 2H 2 O.
Решение : Молярная масса BaCl 2 2H 2 O составляет:
М(BaCl 2 2H 2 O) = 137+ 2 35,5 + 2 18 =244 г/моль
Из формулы BaCl 2 2H 2 O следует, что 1 моль дигидрата хлорида бария содержит 2 моль Н 2 О. Отсюда можно определить массу воды, содержащейся в BaCl 2 2H 2 O:
m(H 2 O) = 2 18 = 36 г.
Находим массовую долю кристаллизационной воды в дигидрате хлорида бария BaCl 2 2H 2 O.
ω(H 2 O) = m(H 2 O)/ m(BaCl 2 2H 2 O) = 36/244 = 0,1475 = 14,75%.
4. Из образца горной породы массой 25 г, содержащей минерал аргентит Ag 2 S, выделено серебро массой 5,4 г. Определите массовую долю аргентита в образце.
Дано : m(Ag)=5,4 г; m = 25 г.
Найти : ω(Ag 2 S) =?
Решение : определяем количество вещества серебра, находящегося в аргентите: ν(Ag) =m(Ag)/M(Ag) = 5,4/108 = 0,05 моль.
Из формулы Ag 2 S следует, что количество вещества аргентита в два раза меньше количества вещества серебра. Определяем количество вещества аргентита:
ν(Ag 2 S)= 0,5 ν (Ag) = 0,5 0,05 = 0,025 моль
Рассчитываем массу аргентита:
m(Ag 2 S) = ν(Ag 2 S) М(Ag 2 S) = 0,025 248 = 6,2 г.
Теперь определяем массовую долю аргентита в образце горной породы, массой 25 г.
ω(Ag 2 S) = m(Ag 2 S)/ m = 6,2/25 = 0,248 = 24,8%.
Вывод формул соединений
5. Определите простейшую формулу соединения калия с марганцем и кислородом, если массовые доли элементов в этом веществе составляют соответственно 24,7, 34,8 и 40,5%.
Дано : ω(K) =24,7%; ω(Mn) =34,8%; ω(O) =40,5%.
Найти : формулу соединения.
Решение : для расчетов выбираем массу соединения, равную 100 г, т.е. m=100 г. Массы калия, марганца и кислорода составят:
m (К) = m ω(К); m (К) = 100 0,247= 24,7 г;
m (Mn) = m ω(Mn); m (Mn) =100 0,348=34,8 г;
m (O) = m ω(O); m (O) = 100 0,405 = 40,5 г.
Определяем количества веществ атомных калия, марганца и кислорода:
ν(К)= m(К)/ М(К) = 24,7/39= 0,63 моль
ν(Mn)= m(Mn)/ М(Mn) = 34,8/ 55 = 0,63 моль
ν(O)= m(O)/ М(O) = 40,5/16 = 2,5 моль
Находим отношение количеств веществ:
ν(К) : ν(Mn) : ν(O) = 0,63: 0,63: 2,5.
Разделив правую часть равенства на меньшее число (0,63) получим:
ν(К) : ν(Mn) : ν(O) = 1: 1: 4.
Следовательно, простейшая формула соединения KMnO 4 .
6. При сгорании 1,3 г вещества образовалось 4,4 г оксида углерода (IV) и 0,9 г воды. Найти молекулярную формулу вещества, если его плотность по водороду равна 39.
Дано : m(в-ва) =1,3 г; m(СО 2)=4,4 г; m(Н 2 О)=0,9 г; Д Н2 =39.
Найти : формулу вещества.
Решение : Предположим, что искомое вещество содержит углерод, водород и кислород, т.к. при его сгорании образовались СО 2 и Н 2 О. Тогда необходимо найти количества веществ СО 2 и Н 2 О, чтобы определить количества веществ атомарных углерода, водорода и кислорода.
ν(СО 2) = m(СО 2)/ М(СО 2) = 4,4/44 = 0,1 моль;
ν(Н 2 О) = m(Н 2 О)/ М(Н 2 О) = 0,9/18 = 0,05 моль.
Определяем количества веществ атомарных углерода и водорода:
ν(С)= ν(СО 2); ν(С)=0,1 моль;
ν(Н)= 2 ν(Н 2 О); ν(Н)= 2 0,05 = 0,1 моль.
Следовательно, массы углерода и водорода будут равны:
m(С) = ν(С) М(С) = 0,1 12 = 1,2 г;
m(Н) = ν(Н) М(Н) = 0,1 1 =0,1 г.
Определяем качественный состав вещества:
m(в-ва) = m(С) + m(Н) = 1,2 + 0,1 = 1,3 г.
Следовательно, вещество состоит только из углерода и водорода (см. условие задачи). Определим теперь его молекулярную массу, исходя из данной в условии задачи плотности вещества по водороду.
М(в-ва) = 2 Д Н2 = 2 39 = 78 г/моль.
ν(С) : ν(Н) = 0,1: 0,1
Разделив правую часть равенства на число 0,1, получим:
ν(С) : ν(Н) = 1: 1
Примем число атомов углерода (или водорода) за «х», тогда, умножив «х» на атомные массы углерода и водорода и приравняв эту сумму молекулярной массе вещества, решим уравнение:
12х + х = 78. Отсюда х= 6. Следовательно, формула вещества С 6 Н 6 – бензол.
Молярный объем газов. Законы идеальных газов. Объемная доля .
Молярный объем газа равен отношению объема газа к количеству вещества этого газа, т.е.
V m = V(X)/ ν(x),
где V m – молярный объем газа - постоянная величина для любого газа при данных условиях; V(X) – объем газа Х; ν(x) – количество вещества газа Х. Молярный объем газов при нормальных условиях (нормальном давлении р н = 101 325 Па ≈ 101,3 кПа и температуре Тн= 273,15 К ≈ 273 К) составляет V m = 22,4 л/моль.
В расчетах, связанных с газами, часто приходится переходить от данных условий к нормальным или наоборот. При этом удобно пользоваться формулой, следующей из объединенного газового закона Бойля-Мариотта и Гей-Люссака:
──── = ─── (3)
Где p – давление; V – объем; Т- температура в шкале Кельвина; индекс «н» указывает на нормальные условия.
Состав газовых смесей часто выражают при помощи объемной доли – отношения объема данного компонента к общему объему системы, т.е.
где φ(Х) – объемная доля компонента Х; V(X) – объем компонента Х; V - объем системы. Объемная доля – безразмерная величина, её выражают в долях от единицы или в процентах.
7. Какой объем займет при температуре 20 о С и давлении 250 кПа аммиак массой 51 г?
Дано : m(NH 3)=51 г; p=250 кПа; t=20 o C.
Найти : V(NH 3) =?
Решение : определяем количество вещества аммиака:
ν(NH 3) = m(NH 3)/ М(NH 3) = 51/17 = 3 моль.
Объем аммиака при нормальных условиях составляет:
V(NH 3) = V m ν(NH 3) = 22,4 3 = 67,2 л.
Используя формулу (3), приводим объем аммиака к данным условиям [температура Т= (273 +20)К = 293 К]:
p н TV н (NH 3) 101,3 293 67,2
V(NH 3) =──────── = ───────── = 29,2 л.
8. Определите объем , который займет при нормальных условиях газовая смесь, содержащая водород, массой 1,4 г и азот, массой 5,6 г.
Дано : m(N 2)=5,6 г; m(H 2)=1,4 ; н.у.
Найти : V(смеси)=?
Решение : находим количества вещества водорода и азота:
ν(N 2) = m(N 2)/ М(N 2) = 5,6/28 = 0,2 моль
ν(H 2) = m(H 2)/ М(H 2) = 1,4/ 2 = 0,7 моль
Так как при нормальных условиях эти газы не взаимодействуют между собой, то объем газовой смеси будет равен сумме объемов газов, т.е.
V(смеси)=V(N 2) + V(H 2)=V m ν(N 2) + V m ν(H 2) = 22,4 0,2 + 22,4 0,7 = 20,16 л.
Расчеты по химическим уравнениям
Расчеты по химическим уравнениям (стехиометрические расчеты) основаны на законе сохранения массы веществ. Однако в реальных химических процессах из-за неполного протекания реакции и различных потерь веществ масса образующихся продуктов часто бывает меньше той, которая должна образоваться в соответствии с законом сохранения массы веществ. Выход продукта реакции (или массовая доля выхода) – это выраженное в процентах отношение массы реально полученного продукта к его массе, которая должна образоваться в соответствии с теоретическим расчетом, т.е.
η = /m(X) (4)
Где η– выход продукта, %; m p (X) - масса продукта Х, полученного в реальном процессе; m(X) – рассчитанная масса вещества Х.
В тех задачах, где выход продукта не указан, предполагается, что он – количественный (теоретический), т.е. η=100%.
9. Какую массу фосфора надо сжечь для получения оксида фосфора (V) массой 7,1 г?
Дано : m(P 2 O 5)=7,1 г.
Найти : m(Р) =?
Решение : записываем уравнение реакции горения фосфора и расставляем стехиометрические коэффициенты.
4P+ 5O 2 = 2P 2 O 5
Определяем количество вещества P 2 O 5 , получившегося в реакции.
ν(P 2 O 5) = m(P 2 O 5)/ М(P 2 O 5) = 7,1/142 = 0,05 моль.
Из уравнения реакции следует, что ν(P 2 O 5)= 2 ν(P), следовательно, количество вещества фосфора, необходимого в реакции равно:
ν(P 2 O 5)= 2 ν(P) = 2 0,05= 0,1 моль.
Отсюда находим массу фосфора:
m(Р) = ν(Р) М(Р) = 0,1 31 = 3,1 г.
10. В избытке соляной кислоты растворили магний массой 6 г и цинк массой 6,5 г. Какой объем водорода, измеренный при нормальных условиях, выделится при этом?
Дано : m(Mg)=6 г; m(Zn)=6,5 г; н.у.
Найти : V(H 2) =?
Решение : записываем уравнения реакции взаимодействия магния и цинка с соляной кислотой и расставляем стехиометрические коэффициенты.
Zn + 2 HCl = ZnCl 2 + H 2
Mg + 2 HCl = MgCl 2 + H 2
Определяем количества веществ магния и цинка, вступивших в реакцию с соляной кислотой.
ν(Mg) = m(Mg)/ М(Mg) = 6/24 = 0,25 моль
ν(Zn) = m(Zn)/ М(Zn) = 6,5/65 = 0,1 моль.
Из уравнений реакции следует, что количество вещества металла и водорода равны, т.е. ν(Mg) = ν(Н 2); ν(Zn) = ν(Н 2), определяем количество водорода, получившегося в результате двух реакций:
ν(Н 2) = ν(Mg) + ν(Zn) = 0,25 + 0,1= 0,35 моль.
Рассчитываем объем водорода, выделившегося в результате реакции:
V(H 2) = V m ν(H 2) = 22,4 0,35 = 7,84 л.
11. При пропускании сероводорода объемом 2,8 л (нормальные условия) через избыток раствора сульфата меди (II) образовался осадок массой 11,4 г. Определите выход продукта реакции.
Дано : V(H 2 S)=2,8 л; m(осадка)= 11,4 г; н.у.
Найти : η =?
Решение : записываем уравнение реакции взаимодействия сероводорода и сульфата меди (II).
H 2 S + CuSO 4 = CuS ↓+ H 2 SO 4
Определяем количество вещества сероводорода, участвующего в реакции.
ν(H 2 S) = V(H 2 S) / V m = 2,8/22,4 = 0,125 моль.
Из уравнения реакции следует, что ν(H 2 S) = ν(СuS) = 0,125 моль. Значит можно найти теоретическую массу СuS.
m(СuS) = ν(СuS) М(СuS) = 0,125 96 = 12 г.
Теперь определяем выход продукта, пользуясь формулой (4):
η = /m(X)= 11,4 100/ 12 = 95%.
12. Какая масса хлорида аммония образуется при взаимодействии хлороводорода массой 7,3 г с аммиаком массой 5,1 г? Какой газ останется в избытке? Определите массу избытка.
Дано : m(HCl)=7,3 г; m(NH 3)=5,1 г.
Найти : m(NH 4 Cl) =? m(избытка) =?
Решение : записываем уравнение реакции.
HCl + NH 3 = NH 4 Cl
Эта задача на «избыток» и «недостаток». Рассчитываем количества вещества хлороводорода и аммиака и определяем, какой газ находится в избытке.
ν(HCl) = m(HCl)/ М(HCl) = 7,3/36,5 = 0,2 моль;
ν(NH 3) = m(NH 3)/ М(NH 3) = 5,1/ 17 = 0,3 моль.
Аммиак находится в избытке, поэтому расчет ведем по недостатку, т.е. по хлороводороду. Из уравнения реакции следует, что ν(HCl) = ν(NH 4 Cl) = 0,2 моль. Определяем массу хлорида аммония.
m(NH 4 Cl) = ν(NH 4 Cl) М(NH 4 Cl) = 0,2 53,5 = 10,7 г.
Мы определили, что аммиак находится в избытке (по количеству вещества избыток составляет 0,1 моль). Рассчитаем массу избытка аммиака.
m(NH 3) = ν(NH 3) М(NH 3) = 0,1 17 = 1,7 г.
13. Технический карбид кальция массой 20 г обработали избытком воды, получив ацетилен, при пропускании которого через избыток бромной воды образовался 1,1,2,2 –тетрабромэтан массой 86,5 г. Определите массовую долю СаС 2 в техническом карбиде.
Дано : m = 20 г; m(C 2 H 2 Br 4)=86,5 г.
Найти : ω(СаC 2) =?
Решение : записываем уравнения взаимодействия карбида кальция с водой и ацетилена с бромной водой и расставляем стехиометрические коэффициенты.
CaC 2 +2 H 2 O = Ca(OH) 2 + C 2 H 2
C 2 H 2 +2 Br 2 = C 2 H 2 Br 4
Находим количество вещества тетрабромэтана.
ν(C 2 H 2 Br 4) = m(C 2 H 2 Br 4)/ М(C 2 H 2 Br 4) = 86,5/ 346 = 0,25 моль.
Из уравнений реакций следует, что ν(C 2 H 2 Br 4) =ν(C 2 H 2) = ν(СаC 2) =0,25 моль. Отсюда мы можем найти массу чистого карбида кальция (без примесей).
m(СаC 2) = ν(СаC 2) М(СаC 2) = 0,25 64 = 16 г.
Определяем массовую долю СаC 2 в техническом карбиде.
ω(СаC 2) =m(СаC 2)/m = 16/20 = 0,8 = 80%.
Растворы. Массовая доля компонента раствора
14. В бензоле объемом 170 мл растворили серу массой 1,8 г. Плотность бензола равна 0,88 г/мл. Определите массовую долю серы в растворе.
Дано : V(C 6 H 6) =170 мл; m(S) = 1,8 г; ρ(С 6 C 6)=0,88 г/мл.
Найти : ω(S) =?
Решение : для нахождения массовой доли серы в растворе необходимо рассчитать массу раствора. Определяем массу бензола.
m(С 6 C 6) = ρ(С 6 C 6) V(C 6 H 6) = 0,88 170 = 149,6 г.
Находим общую массу раствора.
m(р-ра) = m(С 6 C 6) + m(S) =149,6 + 1,8 = 151,4 г.
Рассчитаем массовую долю серы.
ω(S) =m(S)/m=1,8 /151,4 = 0,0119 = 1,19 %.
15. В воде массой 40 г растворили железный купорос FeSO 4 7H 2 O массой 3,5 г. Определите массовую долю сульфата железа (II) в полученном растворе.
Дано : m(H 2 O)=40 г; m(FeSO 4 7H 2 O)=3,5 г.
Найти : ω(FeSO 4) =?
Решение : найдем массу FeSO 4 содержащегося в FeSO 4 7H 2 O. Для этого рассчитаем количество вещества FeSO 4 7H 2 O.
ν(FeSO 4 7H 2 O)=m(FeSO 4 7H 2 O)/М(FeSO 4 7H 2 O)=3,5/278=0,0125моль
Из формулы железного купороса следует, что ν(FeSO 4)= ν(FeSO 4 7H 2 O)=0,0125 моль. Рассчитаем массу FeSO 4:
m(FeSO 4) = ν(FeSO 4) М(FeSO 4) = 0,0125 152 = 1,91 г.
Учитывая, что масса раствора складывается из массы железного купороса (3,5 г) и массы воды (40 г), рассчитаем массовую долю сульфата железа в растворе.
ω(FeSO 4) =m(FeSO 4)/m=1,91 /43,5 = 0,044 =4,4 %.
Задачи для самостоятельного решения
- На 50 г йодистого метила в гексане подействовали металлическим натрием, при этом выделилось 1,12 л газа, измеренного при нормальных условиях. Определите массовую долю йодистого метила в растворе. Ответ : 28,4%.
- Некоторый спирт подвергли окислению, при этом образовалась одноосновная карбоновая кислота. При сжигании 13,2 г этой кислоты получили углекислый газ, для полной нейтрализации которого потребовалось 192 мл раствора КОН с массовой долей 28%. Плотность раствора КОН равна 1,25 г/мл. Определите формулу спирта. Ответ : бутанол.
- Газ, полученный при взаимодействии 9,52 г меди с 50 мл 81 % раствора азотной кислоты, плотностью 1,45 г/мл, пропустили через 150 мл 20 % раствора NaOH плотностью 1,22 г/мл. Определите массовые доли растворенных веществ. Ответ : 12,5% NaOH; 6,48% NaNO 3 ; 5,26% NaNO 2 .
- Определите объем выделившихся газов при взрыве 10 г нитроглицерина. Ответ : 7,15 л.
- Образец органического вещества массой 4,3 г сожгли в кислороде. Продуктами реакции являются оксид углерода (IV) объемом 6,72 л (нормальные условия) и вода массой 6,3 г. Плотность паров исходного вещества по водороду равна 43. Определите формулу вещества. Ответ : С 6 Н 14 .
Закон сохранения массы веществ, открытый М. В. Ломоносовым в 1748 г., гласит:
Материальными носителями массы веществ являются атомы химических элементов, из которых состоят как вступившие в реакцию вещества (реагенты), так и образовавшиеся в результате её новые вещества (продукты реакции). Поскольку при химических реакциях атомы не образуются и не разрушаются, а происходит лишь их перегруппировка, то становится очевидным справедливость открытого М. В. Ломоносовым и подтверждённого позднее А. Лавуазье закона.
В справедливости закона сохранения массы веществ можно легко убедиться на простом опыте. Поместим в колбу немного красного фосфора, закроем её пробкой и взвесим на весах (рис. 96). Затем колбу осторожно нагреем. О том, что произошла химическая реакция, можно определить по появлению в колбе густого белого дыма, состоящего из оксида фосфора (V), который образовался при взаимодействии фосфора с кислородом. При повторном взвешивании колбы с продуктами этой реакции мы убедимся, что масса веществ в колбе не изменилась, хотя и произошло превращение фосфора в его оксид.
Рис. 96.
Экспериментальная проверка закона сохранения массы веществ:
а - взвешивание колбы с фосфором до реакции; б - горение фосфора в закрытой колбе; в - взвешивание колбы с продуктом реакции
Этот же вывод будет нами сделан и при проведении ещё одного простого, но очень наглядного опыта. В специальный сосуд нальём отдельно соляную кислоту и раствор щёлочи, например гидроксида натрия (рис. 97). К раствору щёлочи добавим несколько капель индикатора - фенолфталеина, отчего раствор окрасится в малиновый цвет. Закроем прибор пробкой, уравновесим гирями на весах, отметим массу, а затем сольём растворы. Малиновая окраска исчезнет, потому что кислота и щёлочь прореагировали друг с другом. Масса же сосуда с полученными продуктами реакции не изменилась.

Рис. 97.
Опыт, подтверждающий закон сохранения массы вещества
Аналогичное наблюдение сделал и автор закона сохранения массы веществ М. В. Ломоносов, который проводил опыты в запаянных стеклянных сосудах, «дабы исследовать, прибывает ли вес металла от чистого жару», и обнаружил, что «без пропущения внешнего воздуха вес металлов остаётся в одной мере».
На основании этого закона пишут химические предложения, т. е. составляют уравнения химических реакций с помощью химических слов - формул.
В левой части уравнения записывают формулы (формулу) веществ, вступивших в реакцию, соединяя их знаком «плюс». В правой части уравнения записывают формулы (формулу) образующихся веществ, также соединённых знаком «плюс». Между частями уравнения ставят стрелку. Затем находят коэффициенты - числа, стоящие перед формулами веществ, чтобы число атомов одинаковых элементов в левой и правой частях уравнения было равным.
Запишем, например, уравнение реакции водорода с кислородом. Сначала составим схему реакции - укажем формулы веществ, вступающих в реакцию (водород Н 2 и кислород O 2) и образующихся в результате её (вода Н 2 O), и соединим их стрелкой:
Н 2 + O 2 → Н 2 O (рис. 98, а).

Рис. 98.
Составление уравнения реакции взаимодействия водорода и кислорода
Так как число атомов кислорода в левой части вдвое больше, чем в правой, запишем перед формулой воды коэффициент 2:
Н 2 + O 2 → 2Н 2 O (рис. 98, б).
Но теперь в правой части уравнения стало четыре атома водорода, а в левой их осталось два. Чтобы уравнять число атомов водорода, запишем перед его формулой в левой части коэффициент 2. Так как мы уравняли число атомов каждого элемента в левой и правой частях уравнения, заменим стрелку на знак равенства:
2Н 2 + O 2 = 2Н 2 O (рис. 98, в).
Теперь, наверное, вам понятно, почему такую запись называют уравнением (рис. 99).

Рис. 99.
Закон сохранения массы веществ на примере реакции, уравнение которой 2Н 2 + O 2 = 2Н 2 O
Для составления уравнений химических реакций, кроме знания формул реагентов и продуктов реакции, необходимо верно подобрать коэффициенты.
Это можно сделать, используя несложные правила,
1. Перед формулой простого вещества можно записывать дробный коэффициент, который показывает количество вещества реагирующих и образующихся веществ.
Так, для рассмотренного выше примера:
Н 2 + O 2 → Н 2 O
число атомов кислорода в правой и левой частях уравнения можно сделать равными с помощью коэффициента 1/2, поставив его перед формулой кислорода:
H 2 + 1/2O 2 = H 2 O
Но так как коэффициент показывает не только количество вещества, но и число молекул (атомов), а половину молекулы взять невозможно, лучше переписать приведённое уравнение, удвоив все коэффициенты в нём:
2Н 2 + O 2 = 2Н 2 O.
Приведём ещё пример составления уравнения реакции горения этана С 2 Н 6 , содержащегося в природном газе. Известно, что в результате этого процесса образуются углекислый газ и вода. Схема этой реакции:
С 2 Н 6 + O 2 → СO 2 + Н 2 O.
Уравняем число атомов углерода и водорода:
С 2 Н 6 + O 2 → 2СO 2 + ЗН 2 O.
Теперь в правой части уравнения реакции 7 атомов кислорода, а в левой - только 2. Уравняем число атомов кислорода, записав перед формулой 02 коэффициент 3,5 (7:2 = 3,5):
С 2 Н 6 + 3,5O 2 = 2СO 2 + ЗН 2 O.
И наконец, перепишем полученное уравнение реакции, удвоив коэффициенты перед формулами всех участников реакции:
2С 2 Н 6 + 7O 2 = 4СO 2 + 6Н 2 O.
2. Если в схеме реакции есть формула соли, то вначале уравнивают число ионов, образующих соль.
Например, взаимодействие серной кислоты и гидроксида алюминия описывают схемой:
H 2 SO 4 + Аl(OН) 3 → Al 2 (SO 4) 3 + Н 2 O.
Образующаяся в результате реакции соль - сульфат алюминия Al 2 (SO 4) 3 - состоит из ионов алюминия Аl3+ и сульфат-ионов . Уравняем их число, записав перед формулами H 2 SO 4 и Аl(OН) 3 соответственно коэффициенты 3 и 2:
3H 2 SO 4 + 2Аl(OН) 3 → Al 2 (SO 4) 3 + Н 2 O.
Чтобы уравнять число атомов водорода и кислорода, воспользуемся третьим правилом.
3. Если участвующие в реакции вещества содержат водород и кислород, то атомы водорода уравнивают в предпоследнюю очередь, а атомы кислорода - в последнюю.
Следовательно, уравняем число атомов водорода. В левой части схемы реакции 12 атомов водорода, а в правой - только 2, поэтому перед формулой воды запишем коэффициент 6:
3H 2 SO 4 + 2Аl(OН) 3 → Al 2 (SO 4) 3 + 6Н 2 O.
Индикатором верности расстановки коэффициентов является равенство числа атомов кислорода в левой и правой частях уравнения реакции - по 24 атома кислорода. Поэтому заменим стрелку на знак равенства:
3H 2 SO 4 + 2Аl(OН) 3 = Al 2 (SO 4) 3 + 6Н 2 O.
4. Если в схеме реакции имеется несколько формул солей, то необходимо начинать уравнивание с ионов, входящих в состав соли, содержащей большее их число.
Например, взаимодействие растворов фосфата натрия и нитрата кальция описывают схемой:
Na 3 PO 4 + Ca(NO 3) 2 → Ca 3 (PO 4) 2 + NaNO 3 .
Наибольшее число ионов содержит один из продуктов реакции - фосфат кальция Са 3 (РO 4) 2 , поэтому уравнивают ионы, которыми образована эта соль, - Са 2+ и :
2Na 3 PO 4 + 3Ca(NO 3) 2 → Ca 3 (PO 4) 2 + NaNO 3 .
и, наконец, ионы Na + и N0 - 3:
2Na 3 PO 4 + 3Ca(NO 3) 2 → Ca 3 (PO 4) 2 + 6NaNO 3 .
Ключевые слова и словосочетания
- Химические уравнения.
- Правила подбора коэффициентов в уравнениях реакций.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока - сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания

